Organiskās ķīmijas pamati
Materiāli organiskajā ķīmijā
Kas ir organiskā ķīmija?
Organiskā ķīmija pēta organisku molekulu uzbūvi un īpašības, taču mūsdienās ir sarežģīti precīzi definēt, kur ir organiskās ķīmijas robežas un kur sākas neorganiskā ķīmija, bioķīmija vai polimēru ķīmija. Parasti par organiskām molekulām uzskata visas, kurās ir kovalentās oglekļa saites ar oglekli vai citiem nemetāliem un molmasa nav lielāka kā 1500 - 2000 g/mol, ar izņēmumiem. Taču, lai kā arī organisko ķīmiju definētu, pamatā organiskā ķīmija cenšas atbildēt uz šādiem jautājumiem:
- Kāda ir molekulu uzbūve un kādas molekulas ir iespējamas? Kā noteikt un pierādīt molekulu uzbūvi?
- Kā molekulu uzbūve ietekmē fizikālās īpašības?
- Kā molekulas reaģē un kā ietekmēt reaģētspēju? Kā daba veido molekulas?
Taču svarīgākais organiskajā ķīmijā ir – molekulas uzbūve ietekmē molekulas īpašības neatkarīgi no tā, kādā ceļā molekula iegūta, un tas ir spēkā neatkarīgi no organiskās ķīmijas definīcijas un darbojas arī neorganiskajā ķīmijā, polimēru ķīmijā, bioķīmijā un citās nozarēs.
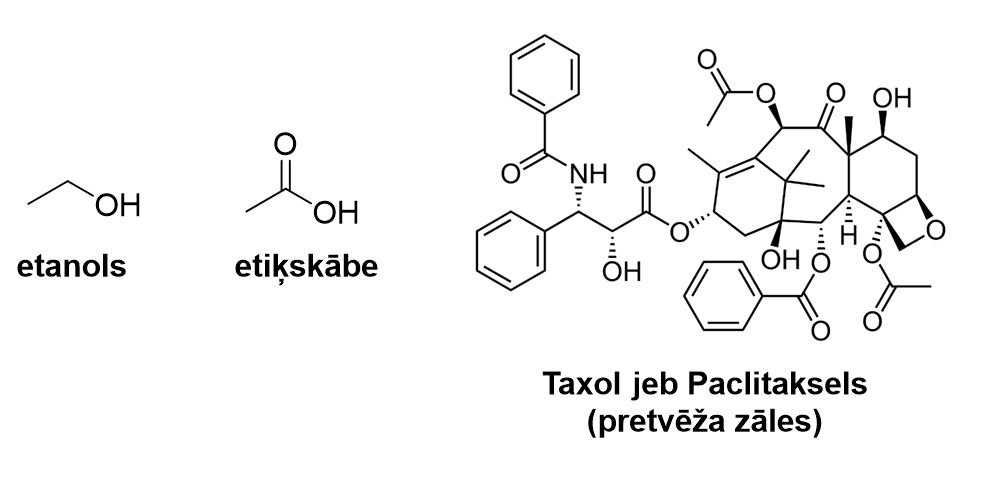
Organiskā sintēze ir lielākā organiskās ķīmijas apakšnodaļa un tās mērķus var apkopot divās daļās: 1) reakcijas produktu iegūšana vai 2) sintēzes reakciju pētīšana.
- Sintēze ir ķīmisko reakciju izmantošana jaunu savienojumu izveidošanai. Jaunus savienojumus nepieciešams veidot, lai radītu jaunas zāles vai izstrādātu jaunus materiālus, kā arī bieži vien sintēzi veic, lai iegūtu līdz šim nebijušas molekulas ar netipiskām īpašībām un pētītu to struktūru jeb uzbūvi.
- Sintēzes reakciju pētīšanu mēdz dēvēt par metodoloģijas izstrādi un to visbiežāk veic, lai izstrādātu pilnīgi jaunas reakcijas, kas ļauj iegūt jaunus savienojumus vai esošus savienojumus īsākā ceļā vai optimizētu esošās sintēzes metodes – sintēzi padarītu lētāku, uzlabotu sintēzes iznākumu (cik procentuāli iegūst vielu no teorētiskā), izmantotu lētākus reaģentus vai tos izmantotu mazākā daudzumā, uzlabotu sintēzes produkta attīrīšanas metodes utt.
Organisko savienojumu pieraksts
Kopš organiskās ķīmijas pirmsākumiem ir eksistējušas dažādas metodes, kā pierakstīt organiskas molekulas, taču modernā literatūrā izmanto tikai vienu – grafisko metodi (attēlā zemāk pēdējā). Šīs metodes priekšrocība pār citām ir tā, ka savienojumu pieraksts ir maksimāli īss un tāds, no kura uzreiz ir skaidrs par molekulas kopējo uzbūvi un saitēm.
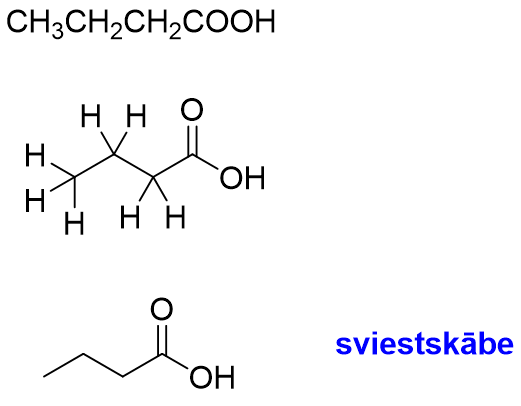
Organisko savienojumu zīmēšanas principi grafiskajā formā:
- Katra ķīmiskā saite ir līnija un līnijas lūzuma vietā atrodas oglekļa atoms (un arī līnijas beigās ir oglekļa atoms). Ja atoms nav ogleklis vai ūdeņradis, tad “lūzuma vietā” norāda ķīmiskā elementa simbolu.
- Jāievēro pareiza ģeometrija ap katru atomu (ņemot vērā atomu hibridizāciju – sp, sp2 vai sp3)
- Saites ar H norāda tikai tad, ja tas saistītas ar heteroatomu. Šādos gadījumos arī bieži starp H un heteroatomu netiek zīmēta saite. Par heteroatomu organiskajā ķīmijā uzskata jebkuru atomu, kas nav C vai H. Turklāt arī C un H izotopus uzskata par heteroatomiem un skaidri jānorāda struktūrās.
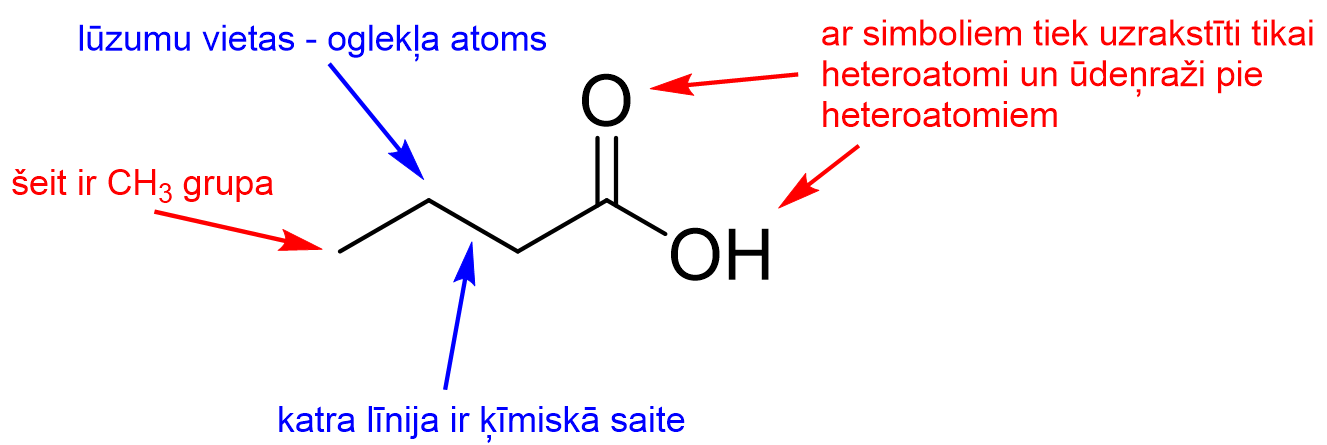
Kāpēc tiek zīmēta oglekļa ķēde kā zig-zags? Rentgentstruktūranalīze ir vienīgā savienojumu analīzes metode, kas ļauj “aplūkot”, kā molekulas patiesībā izskatās un tā tika noteikts, ka tāda arī ir forma, kā garas oglekļa ķēdes izvietojas.
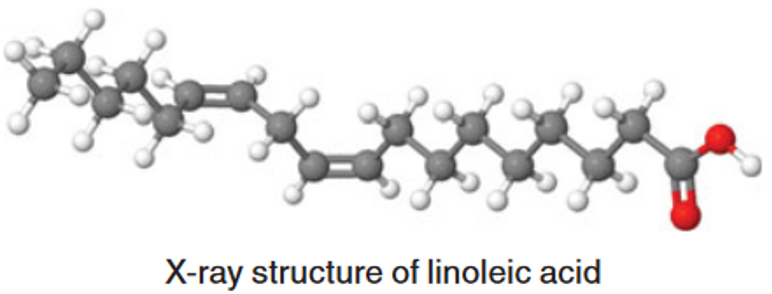
Savienojumu zīmēšanā viena no svarīgākajām lietām ir tos uzzīmēt ar pareiziem leņķiem. Saišu leņķis nosaka atomu hibridizācija: sp3 109.5° (120° 2D attēlojumā), sp2 120° un sp 180°.
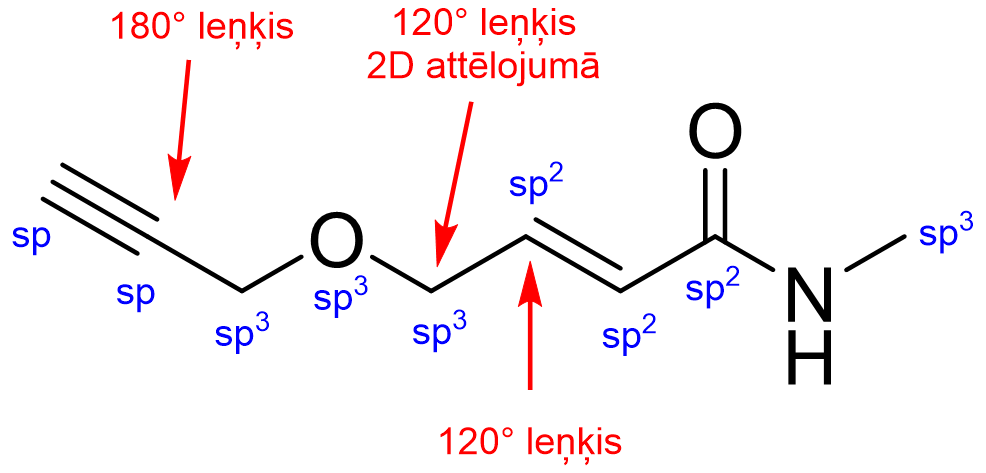
Tā kā ķīmiķi ir diezgan slinki, tad papildus izdomāja, kā vēl varētu vienkāršot savienojumus – izmantot saīsinājumus. Biežāk izmantotie saīsinājumi parādīti attēlā zemāk.
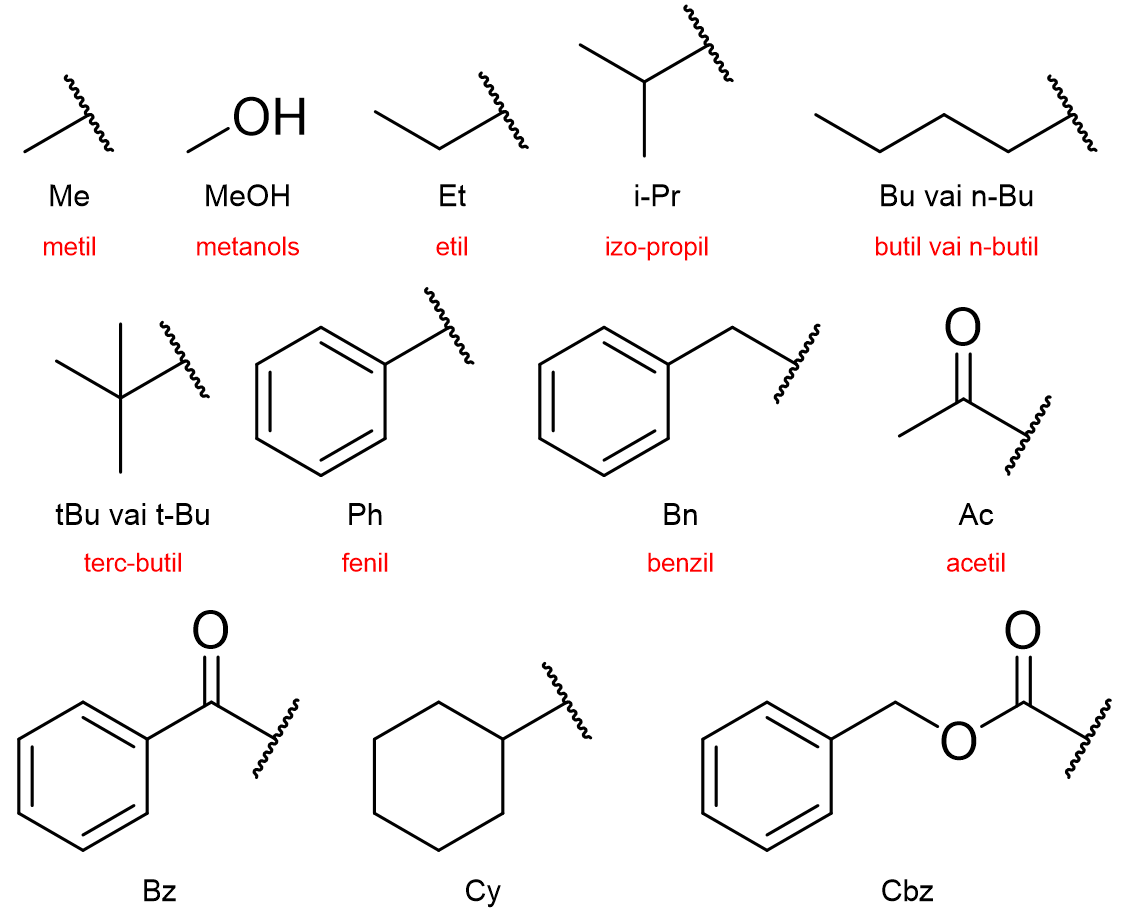
Svarīgākais, ko atcerēties – saīsinājumi vienmēr parāda kāda fragmenta beigas (un nedrīkst būt pa vidu).

Funkcionālās grupas
Bultas organiskajā ķīmijā
Nukleofili un elektrofili
Mehānismi organiskajā ķīmijā
Nukleofila aromātiska aizvietošana
Nukleofila aizvietošana
Pāla-Norra sintēzes (furāns, tiofēns, pirrols)
Pikteta-Špenglera reakcija
Priļežajeva epoksidēšana
Leija-Grifita oksidēšana
Džounsa oksidēšana
Hornera-Vadsvorta-Emmonsa olefinēšana
Gabriela sintēze
Bišlera-Napieraļska reakcija
Brauna hidroborēšana
Koupa eliminēšana
Elektrofilā pievienošana
Diazotēšana
Bērča reducēšana
Bartona dekarboksilēšana
Alkīnu “zipper” jeb rāvējslēdzēja reakcija
Benzoīna kondensācija
Vittiga reakcija
Arbuzova reakcija
Vilsmeijera-Hāka reakcija
Sverna oksidēšana
Štaudingera reakcija
Šapiro reakcija
Reformatska reakcija
Robinsona annulēšana
Pinakola pārgrupēšanās
Ozonolīze
Mitsunobu reakcija
Manniha reakcija
Maikla pievienošanās
Haloforma reakcija
Grinjāra reakcija
Frīdeļa-Kraftsa acilēšana un alkilēšana
Fišera indolu sintēze
Dīlsa-Aldera ciklopievienošanās
Favorska pārgrupēšanās
Desa-Martina oksidēšana
Koupa pārgrupēšanās
Kurtiusa pārgrupēšanās
Klaizena pārgrupēšanās
Klaizena kondensācija
Kanicāro reakcija
Moritas-Bailisa-Hillmana reakcija
Beckmana pārgrupēšanās
Baijera-Villigera oksidēšanās
Arndta-Eišterta homologēšana
